Intervenció nutricional durant la lesió muscular en funció de la fisiopatologia: article de revisió
*Correspondència: Luis Vergara-Gutiérrez luisvergara@medicinadeldeporte.cl
Citació
Vergara-Gutiérrez, L., Lizárraga-Dallo, A., & Pruna-Grive, R. (2020). Nutritional Intervention during Muscle Injury Considering its Pathophysiology: Review Article. Apunts. Educación Física y Deportes, 142, 8-20. https://doi.org/10.5672/apunts.2014-0983.es.(2020/4).142.02
Resum
La lesió genera costos físics, emocionals i econòmics, per la qual cosa s’han buscat estratègies per escurçar al màxim el període de recuperació. Una eina infrautilitzada és la nutricional. Es presenta una revisió de la literatura científica mitjançant una recerca a 4 bases de dades (Pubmed/MEDLINE, Epistemonikos, Embase i Sportdiscus) sobre la fisiopatologia de la lesió muscular i la seva modulació nutricional. Es descriuen canvis locals intervinguts per cèl·lules i mediadors inflamatoris, i canvis secundaris en la composició corporal. Les intervencions nutricionals publicades comprenen l’augment de les proteïnes de la dieta i ajustament de carbohidrats d’acord amb la seva menor despesa energètica. No hi ha estudis que hagin avaluat directament l’ús de suplements durant la lesió, però sí que hi ha evidència indirecta, la majoria favorable, en sarcopènia i recuperació muscular. La intervenció nutricional durant la lesió és fonamental per disminuir les conseqüències negatives de la inactivitat, la qual ha de ser indicada de manera individualitzada.
Introducció
L’aparició d’una lesió és una situació que, si bé es tracta d’evitar, és inherent a la vida de l’esportista. No només involucra costos físics, sinó també emocionals i econòmics, tant pel jugador com per a la institució, com és el cas dels esports (Wall et al., 2014). Se sap que la meitat de les lesions esportives poden considerar-se greus, amb una mitjana d’inactivitat superior a 3 setmanes sense entrenar ni competir (Tipton, 2015). Tota lesió prolongada implica períodes de repòs, generant pèrdua de massa, força i funció muscular (Pierre et al., 2016), pel que tota intervenció per disminuir el període d’immobilitat serà important. D’altra banda, el retorn a la competició pot retardar-se encara més per l’atròfia muscular i l’augment de greix abdominal, el que pot tardar diverses setmanes en resoldre’s. Aquesta acumulació de teixit adipós “no desitjat” s’agreuja per la reducció de la taxa metabòlica local del teixit fet malbé i per una disminució en la sensibilitat del múscul a la insulina (Abadi et al., 2009; Pierre et al., 2016).
Avui dia hi ha diversos tractaments per afavorir i escurçar el període de recuperació, tals com la crioteràpia, massoteràpia, electro estimulació muscular i acupuntura entre d’altres (Dupuy et al., 2018). D’altra banda, s’ha intentat investigar nous tractaments per escurçar la recuperació, com és el cas del plasma ric en plaquetes, anticossos monoclonals que inactiven citocines inflamatòries o la injecció local de factors de creixement entre altres tècniques invasives. Moltes d’aquestes tenen un alt cost, i presenten eventuals complicacions i efectes adversos (Bachl et al., 2009; Mehrabani et al., 2019; Stöllberger i Finsterer, 2019).
Un aspecte poc estudiat, i per moments subestimat, és el factor nutricional. L’alimentació adequada durant el període de la lesió no només pot ajudar a prevenir l’acumulació de greix abdominal, sinó que també podria optimitzar el procés de regeneració dels teixits i disminuir l’atròfia muscular. Des de fa diversos anys que se sap que l’alimentació pot activar o inactivar l’expressió del nostre genoma. Un clar exemple és el de la leucina, un aminoàcid essencial que s’obté dels aliments que és capaç d’activar la via mTOR, activant la síntesi proteica, per la qual cosa és utilitzat per molts esportistes per guanyar massa muscular (Duan et al., 2015; Li et al., 2011). Si fos possible planificar amb l’esportista lesionat una pauta alimentària amb una adequada aportació de proteïnes, aliments amb propietats antiinflamatòries o que fossin capaços de modular la resposta immune, es podria optimitzar el període de recuperació, aconseguint regeneració tissular de millor qualitat en el menor temps possible.
Des de fa segles, moltes cultures han utilitzat aliments amb possibles efectes antiinflamatoris. Tanmateix, en la seva gran majoria manquen d’evidència científica per poder recomanar-ho als esportistes. No només es desconeixen la seva utilitat, sinó també el seu mecanisme d’acció, la dosi adequada o els possibles efectes adversos. És per això que és molt important disposar d’evidència científica de la major qualitat possible per poder recomanar-los amb la seguretat de la seva eficàcia evitant així resultats desfavorables.
En els darrers anys, s’han dut a terme estudis que comproven els efectes immunomoduladors i antiinflamatoris de certs aliments, la majoria d’ells realitzats en pacients amb sarcopènia o en recuperació muscular després d’una sessió d’exercici excèntric (Beaudart et al., 2017; 2018; Chevalley et al., 2010; Colonetti et al., 2016; Cooke et al., 2010; Sousa et al., 2013). La seva aplicació en la medicina de l’esport, específicament durant una lesió esportiva, és una àrea poc desenvolupada, però amb un enorme potencial com a línia futura de recerca, considerant la disminució de costos personals i econòmics que comporta aquesta intervenció. Per aquesta raó, l’objectiu de la present revisió és detallar la fisiopatologia de la lesió muscular en cada una de les seves etapes, per després exposar els aspectes més importants a considerar en el moment de realitzar una intervenció nutricional basada en l’evidència científica disponible.
Metodologia
Estudi descriptiu transversal d’articles publicats mitjançant una revisió narrativa. Es va realitzar una recerca entre febrer i juliol de 2019 a 4 bases de dades (Pubmed/MEDLINE, Epistemonikos, Embase i Sportdiscus) d’articles científics referents a la fisiopatologia de la lesió muscular i la seva intervenció nutricional durant la fase de recuperació. Es van incloure publicacions des de l’inici de la indexació privilegiant la cerca de revisions sistemàtiques i de metanàlisi dels últims 3 anys d’acord amb la classificació de la qualitat de l’evidència vigent en l’actualitat. Es van excloure publicacions que no estiguessin en castellà o anglès, com també aquelles que no estiguessin disponibles en bases de dades electròniques. Inicialment es va realitzar una recerca de paraules clau mitjançant l’eina Mesh com injury, athletic injuries, sports injury, nutrition, muscle regeneration, creatine, protein, whey protein, beta-hydroxy-beta-methylbutyrate, HMB, curcumin, vitamin D, Fatty Acids, Omega-3, Montmorency tart cherry i tart cherry. Posteriorment es va realitzar una nova cerca emprant operadors booleans com : “nutrition” OR “sports nutrition” AND “inj*”, “Athletic Inj*” OR “sports inj*” AND “Sports Nutritional Sciences”, “Athletic Inj*” AND “nutrition”, “muscle Inj*” AND “nutrition”, “protein” AND “athletic Inj*” OR “sports inj*”, “creatine” AND “athletic Inj*” OR “sports inj*”, “curcumin” AND “athletic Inj*” OR “sports inj*”, “Fatty Acids, Omega-3” AND “athletic Inj*” OR “sports inj*”, “vitamin D” AND “athletic Inj*” OR “sports inj*”, “tart cherry” OR “montmorency tart cherry” AND “athletic Inj*” OR “sports inj*”. Es van trobar 21.498 articles, dels quals es van eliminar estudis duplicats i aquells que no corresponien als objectius de l’estudi, resultant finalment 202 publicacions que van ser finalment considerades en la revisió. Als articles de revisió trobats es va recórrer als estudis primaris considerats per l’autoria. En cas de no trobar estudis l’objectiu directe dels quals fos la lesió esportiva, es va buscar la millor evidència indirecta disponible, com la intervenció nutricional en la recuperació de la inflamació muscular, sarcopènia en adults grans o en pacients hospitalitzats després de cirurgies. Un resum de l’estratègia de recerca es mostra a la figura 1.
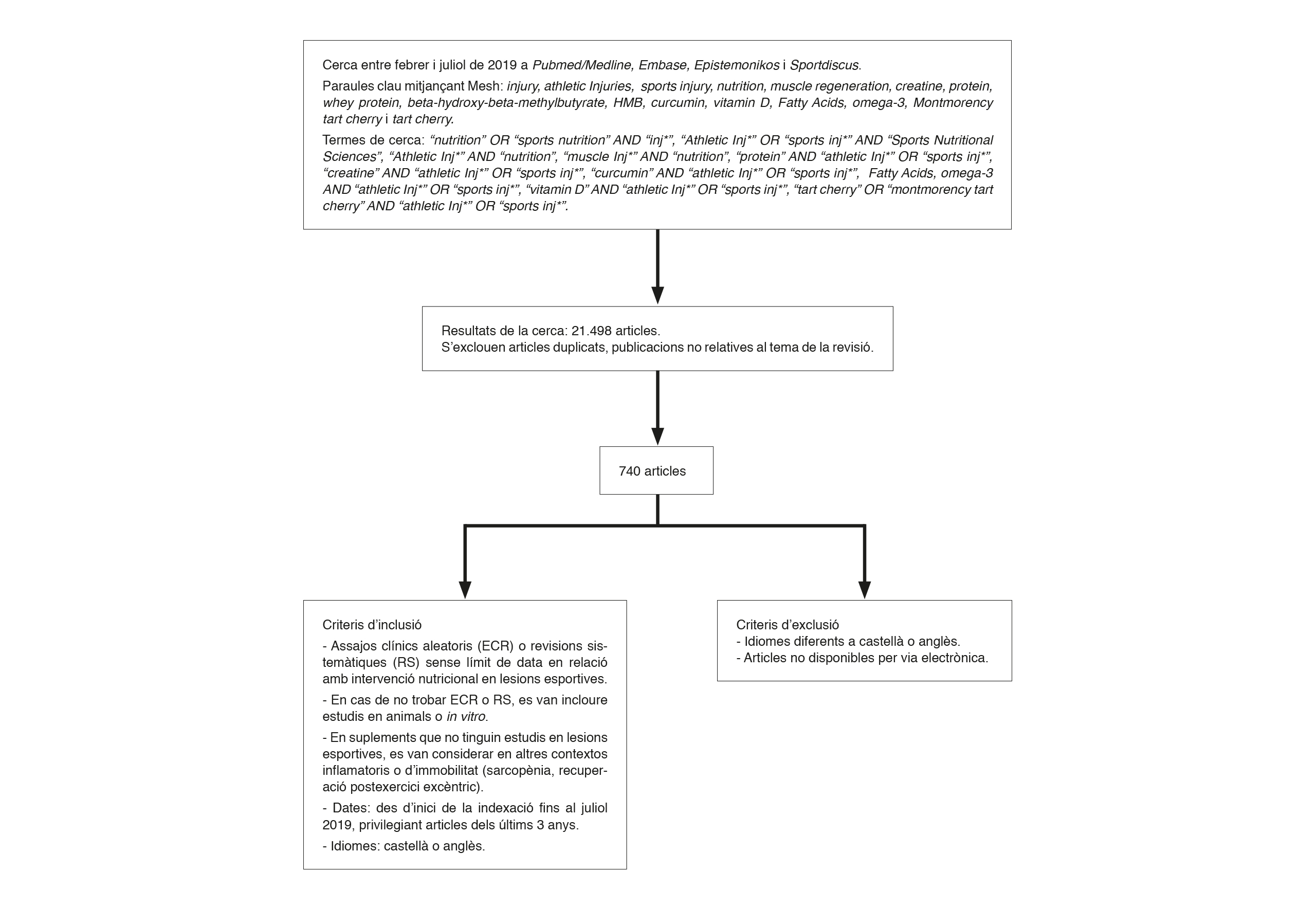
Resultats
No es van trobar revisions sistemàtiques ni assajos clínics aleatoris referents a la intervenció nutricional durant la lesió esportiva, la qual cosa impossibilita la realització de revisions sistemàtiques referents al tema. Només es van trobar 5 revisions narratives del tema (Close et al., 2019; Medina et al.,2014; Tipton, 2010; 2015; Wall et al., 2014), descrivint de manera general possibles intervencions nutricionals durant el període de recuperació. D’altra banda, es van trobar 152 articles relacionats amb suplements que podien ser útils considerant els seus possibles mecanismes d’acció.
Canvis locals al lloc de la lesió muscular
Fisiopatologia de la lesió muscular
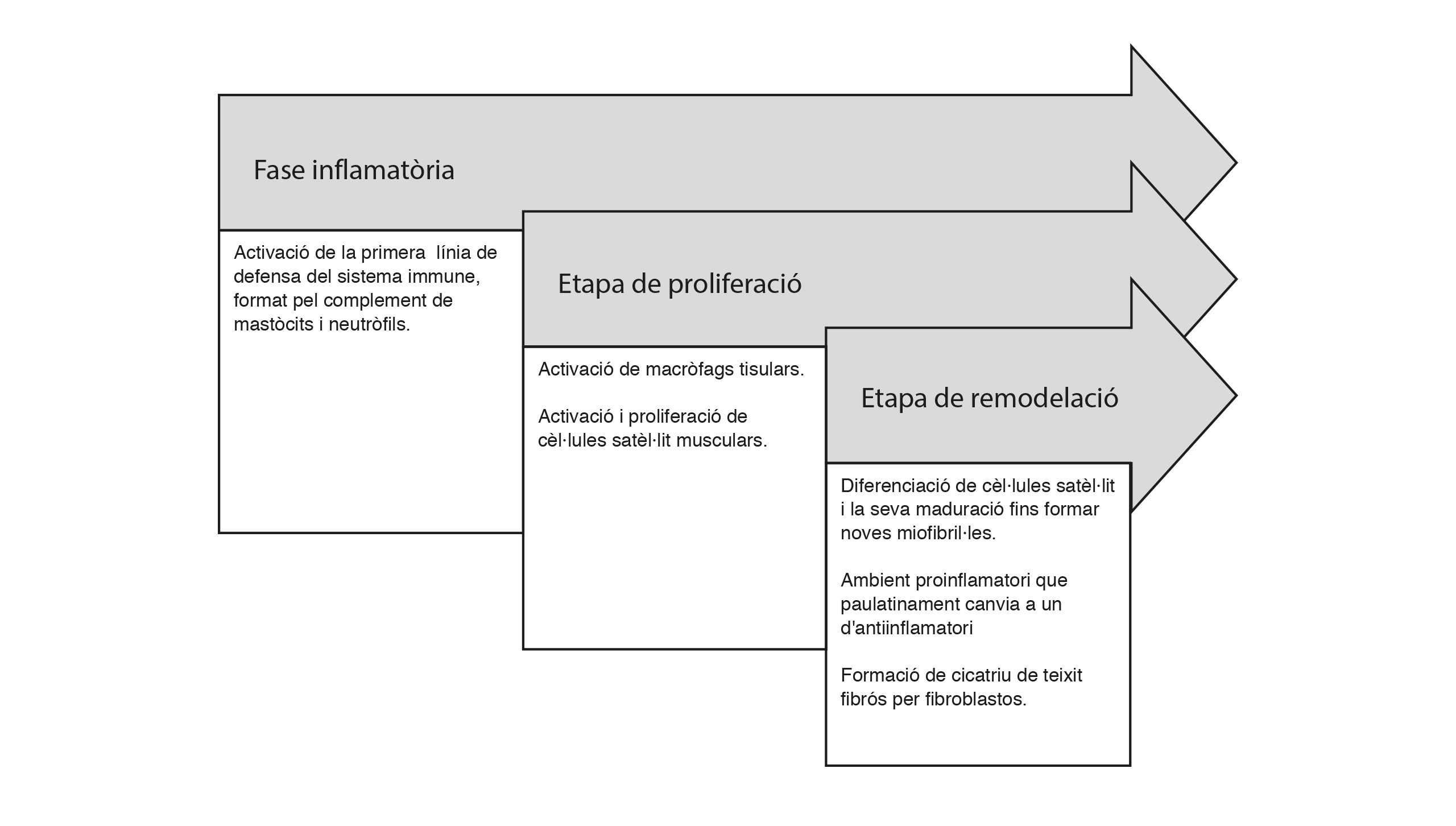
Si bé hi ha diverses classificacions, una de les més utilitzades divideix els canvis de la lesió muscular en tres fases, que se sobreposen, sent difícil poder-ne delimitar l’inici i final ja que ocorren de manera simultània. L’etapa d’inflamació s’inicia des del moment de la lesió fins al setè dia, participant-hi neutròfils, macròfags i limfòcits. La fase de regeneració es considera aproximadament des del segon fins al setè dia, quan hi ha l’activació i proliferació de les cèl·lules satèl·lit (stem cells musculars) que migren i es fusionen amb les fibres musculars. Finalment, hi ha la fase de remodelació que involucra des del cinquè dia fins a la quarta setmana, quan es formen i es regeneren fibres musculars i la matriu extracel·lular (Cheng et al., 2008). Aquestes fases apareixen sintetitzades a la figura 2.
1) Etapa d’inflamació
Immediatament després de produir-se la lesió, s’inicia una resposta inflamatòria, la qual té una durada variable, des d’algunes hores fins a diversos dies depenent del tipus i severitat del mal (Tipton, 2010). La primera etapa del procés de recuperació és anomenada inflamació, i està intervinguda per l’activació del complement, els mastòcits i els neutròfils, que formen part de la primera línia de defensa del sistema immune.

Taula 1
Resum dels articles seleccionats.
Es caracteritza per la necrosi de les fibres danyades, les quals alliberen el seu contingut a l’espai extracel·lular incloent factors quimiotàctics que atreuen les cèl·lules inflamatòries.
El sistema del complement és el primer sensor del dany muscular, i s’activa al cap de pocs segons d’ocorreguda la lesió. La seva activació permet l’arribada de neutròfils i macròfags al dany (Frenette et al., 2000). D’altra banda, també s’activen els mastòcits, la desgranulació dels quals és una de les respostes més precoces del sistema immune innat. Una vegada activades, els mastòcits alliberen citocines inflamatòries, com el factor de necrosi tumoral α (TNF-α), interleucina 1 (IL-1) i histamina, que al seu torn recluten, a més mastòcits, neutròfils i altres cèl·lules inflamatòries (Yang et al., 2018). Finalment, els neutròfils són una de les cèl·lules inflamatòries més importants en etapes precoces després d’una lesió. Igual com els mastòcits, són activats al múscul esquelètic, alliberant citocines inflamatòries com TNF-α, IFN-γ i IL-1β. La seva activació és molt ràpida, envaint les fibres danyades dins de les primeres 2 hores d’ocorregut el dany. El nombre de neutròfils arriba al seu màxim entre 6 i 24 hores després de la lesió i declina ràpidament entre 72 a 96 hores (Arango et al., 2014). Aquests neutròfils temporalment empitjoren el dany muscular i retarden la següent etapa de la regeneració cel·lular en alliberar IL-1 i IL-8 que indueix l’arribada de macròfags al lloc de la inflamació (Yang et al., 2018).
2) Segona etapa. Proliferació
Es caracteritza per l’activació i proliferació de les cèl·lules satèl·lit (stem cells) musculars, associada a l’arribada de macròfags i limfòcits T. Les cèl·lules satèl·lit estan encarregades de la regeneració de les cèl·lules musculars. Es troben ubicades dins de la làmina basal envoltant les miofibres, just entre la membrana basal del múscul i la làmina basal. Són presents a tots els músculs esquelètics i estan associades a tota mena de fibres musculars, però no totes amb igual distribució. Per exemple, el percentatge de cèl·lules satèl·lit al múscul soli adult (fibres lentes) són dues a tres vegades més abundants que al múscul tibial anterior (fibres ràpides). D’altra banda, el seu nombre va disminuint amb el pas dels anys, el que explicaria que la capacitat regenerativa del múscul esquelètic davant d’un dany es redueixi significativament amb l’edat (Järvinen et al., 2005).
Els macròfags són produïts a la medul·la òssia com a monòcits, els quals són reclutats per l’acció dels neutròfils. Comencen a veure’s des de les 24 hores de produïda la lesió incrementant-se 2 dies després, per després minvar ràpidament fins al cinquè dia (Tidball, 2005). Els macròfags juguen un rol primordial en la regulació de la regeneració muscular. Es poden classificar en dos grans grups: els macròfags M1 activats, amb un rol clarament inflamatori, i els M2 també anomenats “alternativament activats”, que són antiinflamatoris (Mantovani et al., 2004). Els macròfags M1 són els dominants durant la inflamació, removent les restes cel·lulars generades pel trauma, gràcies a l’alliberament de citocines com TNF-α, IL-6 i IL-1β. El TNF-α té un important rol en la regeneració muscular. Estudis en laboratori amb ratolins sense aquesta citocina o amb el bloqueig del seu receptor, van mostrar severes alteracions en la regeneració muscular (Chen et al., 2005). El TNF-α pot atreure cèl·lules satèl·lit al lloc de la lesió i promoure la seva proliferació activant el factor nuclear de transcripció kappa β(NfKβ).
La IL-6 és produïda per múltiples cèl·lules inflamatòries, entre les que hi ha els macròfags i els limfòcits T. S’ha vist que és capaç d’estimular la migració, proliferació i diferenciació dels mioblastos. En models animals, amb sobreexpressió de la IL-6, es va veure augmentada l’activació de cèl·lules satèl·lit musculars. D’altra banda, la IL-1β és produïda principalment per macròfags, afavorint l’arribada d’altres macròfags i limfòcits T, estimulant la producció d’IL-6 per les cèl·lules musculars (Yang et al., 2018).
Els limfòcits T són la població cel·lular més gran en ser reclutada a la segona fase de la inflamació. Tant les CD8+ com les CD4+ són atretes pels macròfags M1, apareixent al lloc de lesió al tercer dia i romanent-hi fins al desè (Cheng et al., 2008). Similar als macròfags, els limfòcits T sintetitzen una varietat de factors de creixement i citocines per modular l’ambient inflamatori. Ratolins amb deficiència de limfòcits T mostren alteració en el procés de regeneració, mentre que en incorporar-los poden recuperar el procés regeneratiu (Fu et al., 2015). A més, quan s’apliquen pèptids secretats per limfòcits T humanes s’accelera el procés de regeneració, suggerint que aquestes citocines i factors de creixement secretades pels limfòcits T faciliten la regeneració muscular (Yang et al., 2018).
3) Tercera etapa. Remodelació
En aquesta etapa es desenvolupa la diferenciació de les cèl·lules satèl·lit musculars i la seva maduració fins a formar noves miofibres. L’ambient proinflamatori gradualment es converteix en un d’antiinflamatori, la qual cosa es produeix gràcies al canvi dels macròfags de M1 (proinflamatori) a M2 (antiinflamatori). Els macròfags M2 produeixen citocines antiinflamatòries com les IL-4, IL-10 i IL-13. A més, els macròfags M2 participen en les etapes tardanes de la regeneració muscular. L’absència de macròfags M2 causa retard en el creixement muscular i inhibeix la diferenciació i regeneració del múscul.
Els limfòcits T reguladors són un tipus de limfòcits T. El seu nombre és baix durant les primeres fases de la inflamació, però augmenta bruscament en les etapes tardanes (Fu et al., 2015). Aquests limfòcits T reguladors secreten IL-10 i altres citocines per facilitar la conversió de macròfags M1 a M2.
De manera paral·lela, al lloc de l’hematoma es va formant gradualment una cicatriu de teixit connectiu per acció de fibroblastos, que té per objectiu formar un ancoratge per a les noves miofibril·les en formació. Els fibroblastos són cèl·lules amb un rol molt important en la regeneració tissular, ja que proliferen en estreta relació amb les cèl·lules satèl·lit. L’absència de fibroblastos condueix a una primerenca diferenciació de la cèl·lula satèl·lit evitant la formació de miofibril·les. Malgrat que els fibroblastos són els responsables de la formació de la cicatriu fibrosa, l’estimulació recíproca amb les cèl·lules satèl·lit és molt important per definir si es formarà una nova miofibril·la o es desenvoluparà una indesitjada cicatriu de col·lagen.
A) Canvis secundaris durant una lesió
El període d’inactivitat associat als mediadors inflamatoris existents durant la lesió, genera altres conseqüències que si no són considerades alentiran encara més el retorn a la competició i al nivell de joc existent prèviament.
A.1 Atròfia muscular
Quan l’esportista té una lesió important, en la majoria dels casos hi ha un període inicial d’immobilització o reducció de l’activitat física, anomenada “etapa d’immobilitat o atròfia”, que pot anar des d’uns quants dies fins a diversos mesos. La inactivitat pot ocasionar importants pèrdues a la massa i força musculars, la qual cosa alhora també altera l’estructura i funcionament del tendó. Pèrdues significatives de massa muscular han estat descrites amb només 5 dies d’immobilització. Tanmateix, s’han estudiat canvis en l’expressió gènica dins de les primeres 48 hores de repòs. Aquests canvis a la massa muscular es deuen a un desequilibri entre la síntesi de proteïnes i la seva degradació. Estudis realitzats amb marcadors isotòpics mostren que tant la degradació com la síntesi de proteïnes disminueixen després de 14 dies de repòs estricte al llit, però la síntesi afecta en una proporció superior, generant aquest balanç proteic negatiu (Tipton, 2015).
A.2 Pèrdua de la flexibilitat metabòlica muscular
Es defineix flexibilitat metabòlica com la capacitat de l’organisme per respondre o adaptar-se a les demandes energètiques o metabòliques en una situació determinada. Se l’ha relacionada amb la generació de resistència a la insulina, obesitat i diabetis mellitus tipus 2 (Goodpaster i Sparks, 2017). La funció oxidativa mitocondrial i la flexibilitat metabòlica es veuen afectades durant les primeres setmanes de repòs, en disminuir la transcripció proteica mitocondrial, disminució en les vies de senyalització relacionades amb la biogènesi mitocondrial i un important descens en l’activitat enzimàtica mitocondrial. Alguns d’aquests canvis ja són visibles a les 48 hores d’iniciada la inactivitat. Aquesta disfunció mitocondrial genera un menor transport de glucosa per GLUT4 generant resistència a l’acció de la insulina (Tipton, 2015), la qual cosa també impacta posteriorment en l’acumulació de greix corporal total.
A.3 Resistència anabòlica
Durant aquest període de repòs, associat a la síntesi de mediadors inflamatoris que també es produeix en aquesta etapa, es genera una “resistència anabòlica”, en la qual es redueix la resposta de la síntesi proteica muscular amb els aminoàcids disponibles. Es postula que aquesta resistència anabòlica es podria produir per una digestió i absorció d’aminoàcids alentida, alteració en la perfusió microvascular muscular que alteraria la incorporació d’aminoàcids pel múscul i per un bloqueig en la senyalització molecular anabòlica intracel·lular (Glover et al., 2008).
A.4 Alteracions òssies, tendinoses i lligamentoses
La immobilització no només afecta a la cèl·lula muscular, sinó també a tot el teixit de suport que participa directament i indirectament amb el múscul. Durant la immobilització disminueix la síntesi de col·lagen per part del tendó, canviant les seves propietats mecàniques que són fonamentals per al seu funcionament (Tipton, 2010). Tanmateix, encara s’han d’estudiar els canvis que ocorren en el teixit conjuntiu que envolta la lesió.
A.5 Desregulació de les necessitats energètiques
És evident que, durant l’etapa d’immobilització, com no hi ha ni entrenament ni competició, els requeriments energètics seran menors. Tanmateix, hi ha altres canvis en els requeriments energètics que s’han de considerar. La mateixa cicatrització de la lesió muscular requerirà una demanda energètica local superior, a causa de la necessitat de sintetitzar noves proteïnes per a la recuperació. Aquesta despesa d’energia addicional pot augmentar entre un 15% fins i tot un 50% segons el grau d’inflamació, severitat, mida i durada de la lesió (Tipton, 2015). D’altra banda, si la lesió succeeix en les extremitats inferiors, hi haurà problemes per a la deambulació, pel que serà necessari emprar, amb certa freqüència, bastons o ortesi motiu amb la qual cosa els seus requeriments d’energia per a la deambulació poden augmentar el doble (Tipton, 2015), raó per la qual els nous requeriments energètics de l’esportista lesionat s’han de calcular de manera personalitzada, depenent del tipus de lesió i de la seva activitat diària.
A.6 Resposta psicològica i emocional
Quan hi ha una lesió, l’esportista no només presenta canvis físics, sinó també emocionals. El període de recuperació serà un difícil moment d’ansietat i depressió, amb la incertesa de no conèixer exactament com serà el procés de rehabilitació i les possibles conseqüències en el seu rendiment en tornar a competir. Són comunes les alteracions alimentàries, que poden anar des d’un augment de consum d’aliments rics en calories com també a una restricció excessiva, ambdós amb conseqüències en la seva composició corporal. Un atleta amb símptomes depressius tindrà menys adherència a les indicacions nutricionals de l’equip mèdic, pel que idealment seria important treballar amb un psicòleg esportiu per canviar la percepció de l’esportista davant aquest període.
B) Intervenció nutricional durant la lesió.
La primera intervenció nutricional descrita en la literatura durant el període d’immobilització és evitar els dèficits nutricionals de vitamines, minerals i macronutrients. El macronutrient que més afectaria la recuperació de la lesió serien les proteïnes provinents de la dieta, ja que no només alteraria la síntesi de proteïnes miofibril·lars sinó que també tindria un efecte directe sobre el metabolisme muscular. No existeixen estudis que hagin determinat la quantitat de proteïnes necessàries per evitar l’atròfia muscular específicament durant el període d’inactivitat en lesions d’atletes. Estudis realitzats en homes per Tipton et al. van mostrar que aportar altes dosis de proteïnes (2,3 grams de proteïnes per quilo) va disminuir la pèrdua de massa muscular en períodes de balanç energètic negatiu comparat amb atletes que van rebre 1 gram de proteïnes per quilo al dia. Aquest estudi no es va realitzar en esportistes lesionats sinó en períodes de pèrdua de pes (Tipton, 2015). Se sap que en persones sanes actives, l’aportació de 20 a 25 grams de proteïnes en una dosi maximitza la síntesi proteica i la resistència anabòlica, i la reduïda activitat física fa pensar que seria necessari aportar més quantitat. Aquesta ingesta més gran, que fins ara no s’ha descrit, s’hauria de distribuir al llarg de tot el dia. En el cas dels aminoàcids essencials, tampoc no hi ha treballs en lesions esportives.
La segona intervenció recomanada en la literatura és ajustar els requeriments energètics de l’esportista. És evident que l’esportista lesionat, a causa de la seva inactivitat, gastarà menys calories al dia que un que entrena normalment. Tanmateix, aquest ajustament no és tan simple ja que s’han de considerar altres factors. La cicatrització i la síntesi de proteïnes genera un augment de la despesa energètica que pot augmentar fins i tot un 50% depenent del tipus i severitat de la lesió, sent estimada fins i tot en unes 500 kcal en un home amb una massa muscular important (Tipton, 2015). D’altra banda, cal considerar la despesa secundària a la deambulació: no serà igual un atleta que ha de romandre en repòs complet al llit comparat amb un que requereixi bastons, la qual cosa comporta més despesa energètica. Malgrat l’anàlisi anteriorment exposada, el més freqüent és que l’esportista lesionat, a causa de la seva inactivitat física, empitjori la seva composició corporal, augmentant la seva massa grassa tant abdominal com de les extremitats. S’ha d’assenyalar que no només és important ajustar les calories diàries totals, sinó també la proporció de cadascun dels macronutrients, disminuint els hidrats de carboni i augmentant proporcionalment la ingesta de proteïnes.
Finalment, la tercera intervenció és la utilització de suplements alimentaris, tals com la proteïna del sèrum de llet (Whey Protein), la creatina, l’HMB i antiinflamatoris com la cúrcuma i l’extracte de cirera àcida (tart cherry) entre d’altres. Fins ara no s’han trobat treballs utilitzant aquests suplements en lesions esportives, però si que existeix evidència indirecta de la seva probable utilitat. La proteïna de sèrum de llet i la cúrcuma han mostrat disminuir els marcadors inflamatoris com TNF-α, IL-1α i IL-1β (Derosa et al., 2016; Patel, 2015), pel que podrien ser utilitzats com a immuno moduladors en les primeres etapes de la lesió muscular. Un estudi in vitro va mostrar que l’extracte de cirera àcida pot reduir l’activitat de la COX-2 en un 38.3%, la qual cosa és equivalent a l’efecte d’antiinflamatoris com l’ibuprofèn o el naproxén (Bell et al., 2013). D’altra banda, s’han trobat en estudis in vitro receptors de vitamina D (VDR) en cèl·lules satèl·lit musculars, que són responsables de la regeneració muscular després d’una lesió (Braga et al., 2017).

Taula 2
Evidència dels principals suplements nutricionals.
Si bé hi ha evidència indirecta de l’ús de suplements alimentaris per modular la inflamació muscular, es desconeixen els possibles resultats durant una lesió, ja que se sap que el procés inflamatori és vital per a una adequada regeneració tissular. Per exemple, la COX-2 mitjançant la PGE2 juga un rol en la proliferació de fibroblastos i és un potent regulador del TGF-β1, que alhora participa en la síntesi de col·lagen. S’ha vist, a més, que bloquejar el TNF-α també té efectes negatius en el procés de recuperació, en especial en etapes tardanes del procés (Sass et al., 2018; Tidball, 2005). Per aquesta raó si s’aconseguís saber el moment oportú per disminuir la inflamació sense afectar la qualitat del nou teixit, utilitzant els suplements i/o aliments adequats, es podria modular millor aquest procés. Un exemple seria poder modificar l’activació de macròfags M1 cap a una resposta antiinflamatòria intervinguda per macròfags M2 en lesions cròniques, amb components presents en l’alimentació com la cúrcuma o l’extracte de cirera àcida, el que permetria poder controlar l’excessiva resposta inflamatòria que apareix en certes lesions.
Discussió
Actualment existeixen poques mostres publicades sobre intervencions nutricionals durant el període d’una lesió. La gran majoria dels estudis estan desenvolupats per afavorir la recuperació muscular o prevenir l’osteopènia en adults grans, per la qual cosa la seva aplicabilitat és indirecta. Es requereixen més investigacions realitzades en esportistes joves amb lesions esportives per aplicar millor els resultats.
Una etapa clau en la recuperació d’una lesió és l’etapa inflamatòria, en la que múltiples mediadors inflamatoris, cèl·lules del sistema immunitari i components de la matriu extracel·lular interactuen per iniciar la reparació dels teixits. Aquesta etapa podria modular-se amb aliments antiinflamatoris per escurçar el període de recuperació i d’aquesta manera disminuir costos. Tanmateix, se sap que el procés inflamatori és vital per a una adequada regeneració tissular. Per exemple, s’ha vist que bloquejar el TNF-α també té efectes negatius en el procés de recuperació, en especial en etapes tardanes del procés (Sass et al., 2018; Tidball, 2005). Per aquesta raó, si es descobreix el moment oportú per disminuir la inflamació sense afectar la qualitat del nou teixit, utilitzant els aliments i/o suplements adequats, es podria modular millor aquest procés. Un exemple seria poder modificar l’activació de macròfags M1 cap a una resposta antiinflamatòria intervinguda per macròfags M2 en lesions cròniques, amb components presents en l’alimentació com la curcumina o l’extracte de cirera àcida, llavors es podria controlar l’excessiva resposta inflamatòria que ocorre en certes lesions (taula 3).

Taula 3
Resum dels principals mediadors inflamatoris presents en la recuperació d’una lesió esportiva amb la seva possible modulació nutricional, segons dades actuals.
Un factor molt important i que molts esportistes obliden, és que per tornar a la competició en el menor temps i amb el millor nivell possible no només s’ha de modular la inflamació, sinó que s’ha d’evitar al màxim l’atròfia muscular i l’acumulació de teixit adipós durant el període de recuperació. Mentre s’aconsegueixi menys atròfia i menor augment de greix corporal, més ràpid es podrà recuperar el nivell previ a la lesió. Baixar un excessiu percentatge de greix i enfortir la musculatura pot demorar diverses setmanes i fins i tot mesos, temps addicional que s’afegeix després de l’alta mèdica per una lesió prolongada. Per aconseguir aquests objectius és fonamental ajustar els requeriments energètics de l’esportista, disminuint l’aportació d’hidrats de carboni i augmentant les proteïnes de la dieta per afavorir la recuperació. Aquest ajustament ha de ser individualitzat i adaptat a cada esportista. Una restricció calòrica estricta pot reduir la síntesi proteica entre un 20 a 30% (Tipton, 2015), i això altera la regeneració dels teixits i empitjora l’atròfia muscular. És vital un control periòdic per ajustar la pauta alimentària a mesura que l’esportista augmenti la seva activitat física.
En relació amb l’ús de suplements, no hi ha estudis que avaluïn directament el seu ús en lesions esportives. Com ja es va esmentar, és difícil obtenir conclusions vàlides considerant com d’heterogeni són les dosis, el tipus de pacients i els protocols d’exercici realitzats. D’altra banda, és difícil avaluar l’impacte d’un component aïllat de la dieta considerant la complexitat de controlar el consum d’altres aliments que poden influir en els resultats. S’agrega a l’anterior que les variables mesurades moltes vegades són subjectives, difícils de quantificar, com són el nivell de dolor o el grau de cicatrització d’una ferida. Les dades anteriors obliguen a analitzar cautelosament els resultats dels estudis disponibles, sense treure conclusions definitives i intentar aplicar-les amb criteris determinats en cada cas fins que aparegui una nova evidència científica de millor aplicabilitat.
És important posar èmfasi en el fet que la millor intervenció nutricional és privilegiar una adequada alimentació, afavorint el consum de fruites i verdures. En cas de necessitar incrementar l’aportació diària de proteïnes, es pot fer augmentant-ne el consum des dels aliments. En situacions en què és difícil aportar-ne altes quantitats des de la dieta, com és el cas de la cúrcuma, es poden utilitzar suplements per obtenir nivells plasmàtics adequats d’una manera més fàcil i còmoda.
En els propers anys caldrà dur a terme nous treballs, que estudiïn la relació de l’alimentació amb processos immunitaris i d’inflamació sistèmica. En l’àmbit nutricional, s’han d’obrir noves línies de recerca sobre lesions esportives per determinar quins aliments o suplements estimulen les cèl·lules satèl·lit musculars per regenerar el dany, modulen la resposta inflamatòria afavorint l’activitat antiinflamatòria dels macròfags M2, eviten la formació d’una cicatriu fibrosa i eviten al màxim l’atròfia muscular per immobilitat. A part de la seva utilitat s’han de conèixer també les dosis adequades, el millor moment per a la seva administració i els seus possibles efectes adversos.
Conclusions
Considerant tant la fisiopatologia com els múltiples canvis tan locals com secundaris després d’una lesió esportiva, s’ha de realitzar una intervenció nutricional personalitzada en un atleta amb una lesió de llarga recuperació, depenent de l’etapa de recuperació en la qual es trobi l’esportista. S’han d’ajustar els macronutrients segons els nous requeriments energètics d’un esportista en recuperació, mitjançant una pauta alimentària personalitzada. D’aquesta manera, es podria controlar el procés inflamatori, millorar la qualitat de la regeneració muscular, escurçar el temps de recuperació, reduir al mínim l’atròfia muscular i l’acumulació de greix abdominal, complementant el treball realitzat per fisioterapeutes i readaptadors. Fins ara no hi ha prou evidència científica en l’ús d’aliments i suplements en lesions esportives. Es requereix més recerca que es i dissenyin específicament per a aquest tipus de pacients, per definir l’alimentació i suplementació que són beneficioses, les dosis adequades, el moment oportú i la durada del tractament.
Referències
[1] Abadi, A., Glover, E. I., Isfort, R. J., Raha, S., Safdar, A., Yasuda, N., et al. (2009). Limb Immobilization Induces a Coordinate Down-Regulation of Mitochondrial and Other Metabolic Pathways in Men and Women. PLoS ONE, 4(8), e6518–14. https://doi.org/10.1371/journal.pone.0006518
[2] Arango Duque, G., & Descoteaux, A. (2014). Macrophage cytokines: involvement in immunity and infectious diseases. Frontiers in Immunology, 5(11), 491. https://doi.org/10.3389/fimmu.2014.00491
[3] Bachl, N., Derman, W., Engebretsen, L., Goldspink, G., Kinzlbauer, M., Tschan, H., et al. (2009). Therapeutic use of growth factors in the musculoskeletal system in sports-related injuries. The Journal of Sports Medicine and Physical Fitness, 49(4), 346–357.
[4] Beaudart, C., Dawson, A., Shaw, S. C., Harvey, N. C., Kanis, J. A., Binkley, N., et al. (2017). Nutrition and physical activity in the prevention and treatment of sarcopenia: systematic review. Osteoporosis International, 28(6), 1–17. https://doi.org/10.1007/s00198-017-3980-9
[5] Beaudart, C., Rabenda, V., Simmons, M., Geerinck, A., de Carvalho, I. A., Reginster, J. Y., et al. (2018). Effects of Protein, Essential Amino Acids, B-Hydroxy B-Methylbutyrate, Creatine, Dehydroepiandrosterone and Fatty Acid Supplementation on Muscle Mass, Muscle Strength and Physical Performance in Older People Aged 60 Years and Over. A Systematic Review of the Literature. The Journal of Nutrition, Health & Aging, 22(1), 117–130. https://doi.org/10.1007/s12603-017-0934-z
[6] Bell, P. G., McHugh, M. P., Stevenson, E., & Howatson, G. (2013). The role of cherries in exercise and health. Scandinavian Journal of Medicine & Science in Sports, 24(3), 477–490. https://doi.org/10.1111/sms.12085
[7] Bell, P., Stevenson, E., Davison, G., & Howatson, G. (2016). The Effects of Montmorency Tart Cherry Concentrate Supplementation on Recovery Following Prolonged, Intermittent Exercise. Nutrients, 8(7), 441–11. https://doi.org/10.3390/nu8070441
[8] Braga, M., Simmons, Z., Norris, K. C., Ferrini, M. G., & Artaza, J. N. (2017). Vitamin D induces myogenic differentiation in skeletal muscle derived stem cells. Endocrine Connections, 6(3), 139–150. https://doi.org/10.1530/EC-17-0008
[9] Capó, X., Martorell, M., Sureda, A., Tur, J. A., & Pons, A. (2016). Effects of dietary Docosahexaenoic, training and acute exercise on lipid mediators. Journal of the International Society of Sports Nutrition, 13(1), 1–13. https://doi.org/10.1186/s12970-016-0126-y
[10] Chen, S.-E., Gerken, E., Zhang, Y., Zhan, M., Mohan, R. K., Li, A. S., et al. (2005). Role of TNF-α signaling in regeneration of cardiotoxin-injured muscle. American Journal of Physiology-Cell Physiology, 289(5), C1179–C1187. https://doi.org/10.1152/ajpcell.00062.2005
[11] Cheng, M., Nguyen, M.-H., Fantuzzi, G., & Koh, T. J. (2008). Endogenous interferon-γ is required for efficient skeletal muscle regeneration. American Journal of Physiology-Cell Physiology, 294(5), C1183–C1191. https://doi.org/10.1152/ajpcell.00568.2007
[12] Chevalley, T., Hoffmeyer, P., Bonjour, J.-P., & Rizzoli, R. (2010). Early serum IGF-I response to oral protein supplements in elderly women with a recent hip fracture. Clinical Nutrition, 29(1), 78–83. https://doi.org/10.1016/j.clnu.2009.07.003
[13] Close, G. L., Sale, C., Baar, K., & Bermon, S. (2019). Nutrition for the Prevention and Treatment of Injuries in Track and Field Athletes. International Journal of Sport Nutrition and Exercise Metabolism, 29(2), 189–197. https://doi.org/10.1123/ijsnem.2018-0290
[14] Colonetti, T., Grande, A. J., Milton, K., Foster, C., Alexandre, M. C. M., Uggioni, M. L. R., & Rosa, M. I. D. (2016). Effects of whey protein supplement in the elderly submitted to resistance training: systematic review and meta-analysis. International Journal of Food Sciences and Nutrition, 68(3), 257–264. https://doi.org/10.1080/09637486.2016.1232702
[15] Cooke, M. B., Rybalka, E., Stathis, C. G., Cribb, P. J., & Hayes, A. (2010). Whey protein isolate attenuates strength decline after eccentrically-induced muscle damage in healthy individuals. Journal of the International Society of Sports Nutrition, 7(1), 30–9. https://doi.org/10.1186/1550-2783-7-30
[16] Da Boit, M., Hunter, A. M., & Gray, S. R. (2017). Fit with good fat? The role of n-3 polyunsaturated fatty acids on exercise performance. Metabolism: Clinical and Experimental, 66, 45–54. https://doi.org/10.1016/j.metabol.2016.10.007
[17] Daily, J. W., Yang, M., & Park, S. (2016). Efficacy of Turmeric Extracts and Curcumin for Alleviating the Symptoms of Joint Arthritis: A Systematic Review and Meta-Analysis of Randomized Clinical Trials. Journal of Medicinal Food, 19(8), 717–729. https://doi.org/10.1089/jmf.2016.3705
[18] Delfan, M., Ebrahim, K., Baesi, F., Mirakhori, Z., Ghalamfarsa, G., Bakhshaei, P., et al. (2015). The immunomodulatory effects of fish-oil supplementation in elite paddlers_ A pilot randomized double blind placebo-controlled trial. Prostaglandins Leukotrienes and Essential Fatty Acids, 99(C), 35–40. https://doi.org/10.1016/j.plefa.2015.04.011
[19] Derosa, G., Maffioli, P., Simental-Mendía, L. E., Bo, S., & Sahebkar, A. (2016). Effect of curcumin on circulating interleukin-6 concentrations: A systematic review and meta-analysis of randomized controlled trials. Pharmacological Research, 111, 394–404. https://doi.org/10.1016/j.phrs.2016.07.004
[20] Dreyer, H. C., Strycker, L. A., Senesac, H. A., Hocker, A. D., Smolkowski, K., Shah, S. N., & Jewett, B. A. (2013). Essential amino acid supplementation in patients following total knee arthroplasty. The Journal of Clinical Investigation, 123(11), 4654–4666. https://doi.org/10.1172/JCI70160
[21] Duan, Y., Li, F., Guo, Q., Wang, W., Zhang, L., Wen, C., et al. (2018). β-Hydroxy-β-methyl Butyrate Is More Potent Than Leucine in Inhibiting Starvation-Induced Protein Degradation in C2C12 Myotubes. Journal of Agricultural and Food Chemistry, 66(1), 170–176. https://doi.org/10.1021/acs.jafc.7b04841
[22] Duan, Y., Li, F., Li, Y., Tang, Y., Kong, X., Feng, Z., et al. (2015). The role of leucine and its metabolites in protein and energy metabolism. Amino Acids, 48(1), 41–51. https://doi.org/10.1007/s00726-015-2067-1
[23] Dupuy, O., Douzi, W., Theurot, D., Bosquet, L., & Dugué, B. (2018). An Evidence-Based Approach for Choosing Post-exercise Recovery Techniques to Reduce Markers of Muscle Damage, Soreness, Fatigue, and Inflammation: A Systematic Review With Meta-Analysis. Frontiers in Physiology, 9, 372–15. https://doi.org/10.3389/fphys.2018.00403
[24] Eijnde, B. O. ‘., Ursø, B., Richter, E. A., Greenhaff, P. L., & Hespel, P. (2001). Effect of Oral Creatine Supplementation on Human Muscle GLUT4 Protein Content After Immobilization. Diabetes…, 50(1), 18–23. https://doi.org/10.2337/diabetes.50.1.18
[25] Frenette, J., Cai, B., & Tidball, J. G. (2000). Complement Activation Promotes Muscle Inflammation during Modified Muscle Use. The American Journal of Pathology, 156(6), 2103–2110. https://doi.org/10.1016/S0002-9440(10)65081-X
[26] Fu, X., Xiao, J., Wei, Y., Li, S., Liu, Y., Yin, J., et al. (2015). Combination of inflammation-related cytokines promotes long-term muscle stem cell expansion. Nature Publishing Group, 25(6), 655–673. https://doi.org/10.1038/cr.2015.58
[27] Glover, E. I., Phillips, S. M., Oates, B. R., Tang, J. E., Tarnopolsky, M. A., Selby, A., et al. (2008). Immobilization induces anabolic resistance in human myofibrillar protein synthesis with low and high dose amino acid infusion. The Journal of Physiology, 586(24), 6049–6061. https://doi.org/10.1113/jphysiol.2008.160333
[28] Goodpaster, B. H., & Sparks, L. M. (2017). Metabolic Flexibility in Health and Disease. Cell Metabolism, 25(5), 1027–1036. https://doi.org/10.1016/j.cmet.2017.04.015
[29] Henrotin, Y., Priem, F., & Mobasheri, A. (2013). Curcumin: a new paradigm and therapeutic opportunity for the treatment of osteoarthritis: curcumin for osteoarthritis management. SpringerPlus, 2(1), 56. https://doi.org/10.1186/2193-1801-2-56
[30] Hespel, P., Op’t Eijnde, B., Van Leemputte, M., Ursø, B., Greenhaff, P. L., Labarque, V., et al. (2001). Oral creatine supplementation facilitates the rehabilitation of disuse atrophy and alters the expression of muscle myogenic factors in humans. The Journal of Physiology, 536(Pt 2), 625–633.
[31] Järvinen, T. A. H., Järvinen, T. L. N., Kääriäinen, M., Kalimo, H., & Järvinen, M. (2005). Muscle injuries: biology and treatment. The American Journal of Sports Medicine, 33(5), 745–764. https://doi.org/10.1177/0363546505274714
[32] Karimian, M. S., Matteo Pirro MD, P., Majeed, M., & Amirhossein Sahebkar PharmD, P. (2017). Curcumin as a natural regulator of monocyte chemoattractant protein-1. Cytokine and Growth Factor Reviews, 33, 55–63. doi:10.1016/j.cytogfr.2016.10.001
[33] Levers, K., Dalton, R., Galvan, E., O’Connor, A., Goodenough, C., Simbo, S., et al. (2016). Effects of powdered Montmorency tart cherry supplementation on acute endurance exercise performance in aerobically trained individuals. Journal of the International Society of Sports Nutrition, 1–24. https://doi.org/10.1186/s12970-016-0133-z
[34] Li, F., Yin, Y., Tan, B., Kong, X., & Wu, G. (2011). Leucine nutrition in animals and humans: mTOR signaling and beyond. Amino Acids, 41(5), 1185–1193. https://doi.org/10.1007/s00726-011-0983-2
[35] Liao, C.-D., Tsauo, J.-Y., Wu, Y.-T., Cheng, C.-P., Chen, H.-C., Huang, Y.-C., et al. (2017). Effects of protein supplementation combined with resistance exercise on body composition and physical function in older adults: a systematic review and meta-analysis. The American Journal of Clinical Nutrition, 106(4), 1078–1091. https://doi.org/10.3945/ajcn.116.143594
[36] Mantovani, A., Sica, A., Sozzani, S., Allavena, P., Vecchi, A., & Locati, M. (2004). The chemokine system in diverse forms of macrophage activation and polarization. Trends in Immunology, 25(12), 677–686. https://doi.org/10.1016/j.it.2004.09.015
[37] Medina, D., Lizarraga, A., & Drobnick, F.2014. (s.d.). Injury prevention and nutrition in football. Sports Science Exchange, 27, 1–5.
[38] Mehrabani, D., Seghatchian, J., & Acker, J. P. (2019). Platelet rich plasma in treatment of musculoskeletal pathologies. Transfusion and Apheresis Science, 58(6), 102675–11. https://doi.org/10.1016/j.transci.2019.102675
[39] Minshull, C., Biant, L. C., Ralston, S. H., & Gleeson, N. (2015). A Systematic Review of the Role of Vitamin D on Neuromuscular Remodelling Following Exercise and Injury. Calcified Tissue International, 98(5), 426–437. https://doi.org/10.1007/s00223-015-0099-x
[40] Patel, S. (2015). Functional food relevance of whey protein: A review of recent findings and scopes ahead. Journal of Functional Foods, 19(PA), 308–319. https://doi.org/10.1016/j.jff.2015.09.040
[41] Pierre, N., Appriou, Z., Gratas-Delamarche, A., & Derbré, F. (2016). From physical inactivity to immobilization: Dissecting the role of oxidative stress in skeletal muscle insulin resistance and atrophy. Free Radical Biology and Medicine, 98, 197–207. https://doi.org/10.1016/j.freeradbiomed.2015.12.028
[42] Sahebkar, A. (2013). Are Curcuminoids Effective C-Reactive Protein-Lowering Agents in Clinical Practice? Evidence from a Meta-Analysis. Phytotherapy Research, 28(5), 633–642. https://doi.org/10.1002/ptr.5045
[43] Sahebkar, A., Cicero, A. F. G., Simental-Mendía, L. E., Aggarwal, B. B., & Gupta, S. C. (2016). Curcumin downregulates human tumor necrosis factor-α levels: A systematic review and meta-analysis ofrandomized controlled trials. Pharmacological Research, 107, 234–242. https://doi.org/10.1016/j.phrs.2016.03.026
[44] Sass, F. A., Fuchs, M., Pumberger, M., Geissler, S., Duda, G. N., Perka, C., & Schmidt-Bleek, K. (2018). Immunology Guides Skeletal Muscle Regeneration. International Journal of Molecular Sciences, 19(3). https://doi.org/10.3390/ijms19030835
[45] Schneider, A., Hossain, I., VanderMolen, J., & Nicol, K. (2017). Comparison of remicade to curcumin for the treatment of Crohn’s disease_ A systematic review, 33, 32–38. https://doi.org/10.1016/j.ctim.2017.06.002
[46] Sousa, M., Teixeira, V. H., & Soares, J. (2013). Dietary strategies to recover from exercise-induced muscle damage. International Journal of Food Sciences and Nutrition, 65(2), 151–163. https://doi.org/10.3109/09637486.2013.849662
[47] Stöllberger, C., & Finsterer, J. (2019). Side effects of whole-body electro-myo-stimulation. Wiener Medizinische Wochenschrift (1946), 169(7-8), 173–180. https://doi.org/10.1007/s10354-018-0655-x
[48] Tidball, J. G. (2005). Inflammatory processes in muscle injury and repair. American Journal of Physiology-Regulatory, Integrative and Comparative Physiology, 288(2), R345–R353. https://doi.org/10.1152/ajpregu.00454.2004
[49] Tipton, K. D. (2010). Nutrition for acute exercise-induced injuries. Annals of Nutrition and Metabolism, 57 Suppl 2(s2), 43–53. https://doi.org/10.1159/000322703
[50] Tipton, K. D. (2015). Nutritional Support for Exercise-Induced Injuries. Sports Medicine, 45 Suppl 1(S1), S93–104. https://doi.org/10.1007/s40279-015-0398-4
[51] Wall, B. T., Morton, J. P., & Van Loon, L. J. C. (2014). Strategies to maintain skeletal muscle mass in the injured athlete: Nutritional considerations and exercise mimetics. European Journal of Sport Science, 15(1), 53–62. https://doi.org/10.1080/17461391.2014.936326
[52] Wu, H., Xia, Y., Jiang, J., Du, H., Guo, X., Liu, X., et al. (2015). Effect of beta-hydroxy-beta-methylbutyrate supplementation on muscle loss in older adults: A systematic review and meta-analysis. Archives of Gerontology and Geriatrics, 61(2), 168–175. https://doi.org/10.1016/j.archger.2015.06.020
[53] Yang, W., & Hu, P. (2018). Skeletal muscle regeneration is modulated by inflammation. Journal of Orthopaedic Translation, 13, 1–8. https://doi.org/10.1016/j.jot.2018.01.002
[54] Yoneme, H., Hatakeyama, J., Danjo, A., Oida, H., Yoshinari, M., Aijima, R., et al. (2015). Milk basic protein supplementation enhances fracture healing in mice. Nutrition, 31(2), 399–405. https://doi.org/10.1016/j.nut.2014.08.008
ISSN: 2014-0983
Rebut: 10 de febrer de 2020
Acceptat: 5 de juny de 2020
Publicat: 1 d'octubre de 2020
Editat per: © Generalitat de Catalunya Departament de la Presidència Institut Nacional d’Educació Física de Catalunya (INEFC)
© Copyright Generalitat de Catalunya (INEFC). Aquest article està disponible a la url https://www.revista-apunts.com/. Aquest treball està publicat sota una llicència Internacional de Creative Commons Reconeixement 4.0. Les imatges o qualsevol altre material de tercers d’aquest article estan incloses a la llicència Creative Commons de l’article, tret que s’indiqui el contrari a la línia de crèdit; si el material no s’inclou sota la llicència Creative Commons, els usuaris hauran d’obtenir el permís del titular de la llicència per reproduir el material. Per veure una còpia d’aquesta llicència, visiteu https://creativecommons.org/licenses/by/4.0/deed.ca


